AI創薬の類まれな可能性 最新研究が雨後の筍のように発表されている
創薬はいま最も熱気を帯びている人工知能(AI)の応用分野である。従来の創薬を著しく効率化できる可能性が生じ、それを後押しするような研究が雨後の筍のように出てきている。

創薬はいま最も熱気を帯びている人工知能(AI)の応用分野である。従来の創薬を著しく効率化できる可能性が生じ、それを後押しするような研究が雨後の筍のように出てきている。
生命を救う薬物治療の開発に利用できる潜在的な薬物様特性を持っているのは、いったい何パーセントだろうか? 数百万? 数十億? 数兆個か? 答えは、「10の60乗」である。
創薬研究者は、創薬と呼ばれるプロセスにおいて、特定のタンパク質標的に適切に結合する、あるいは「ドッキング」できる有望な薬物様分子を見つけなければならない。タンパク質とのドッキングに成功すると、リガンドとも呼ばれる結合薬がタンパク質の機能を停止させることができる。もしこれが細菌の必須タンパク質に起これば、細菌を殺すことができ、人体を保護することができる。
しかし、創薬のプロセスには財政的にも計算機的にもコストがかかり、数十億ドルを注ぎ込み、食品医薬品局(FDA)からの最終承認までに10年以上の開発・試験期間が必要だ。さらに、全薬剤の90%は、ヒトで試験された後、効果がなかったり、副作用が多すぎたりして失敗している。製薬会社は、この失敗のコストを回収するために、成功した薬の価格を上げるという方法をとっている。
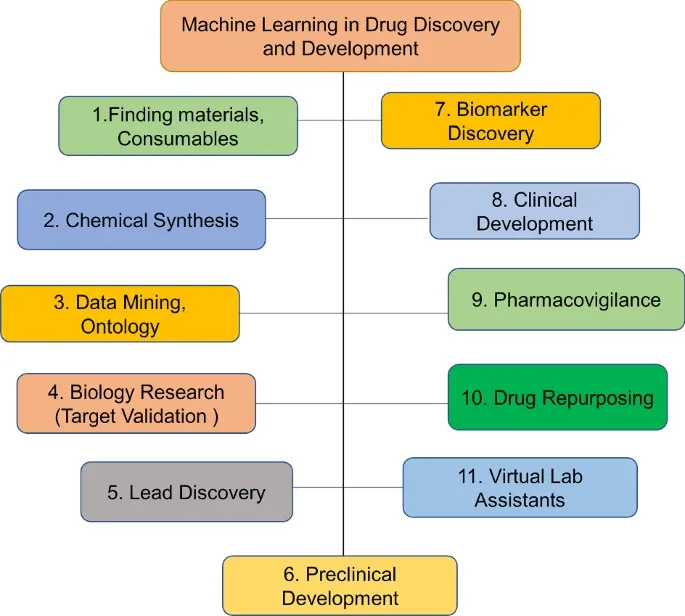
機械学習(ML)アプローチは、豊富で高品質なデータで十分に特定された質問に対する発見と意思決定を改善できる一連のツールを提供する。MLを適用する機会は、創薬のすべての段階に存在するのだ。例えば、ターゲットバリデーション(創薬の標的として適当な分子を選定すること)、予後バイオマーカー(治療の有無にかかわらず予後に影響を及ぼす因子)の同定、臨床試験におけるデジタル病理データの解析などである。
AI創薬を加速させる研究は雨後の筍ように出てきている。マサチューセッツ工科大学(MIT)の研究者たちは、今月17〜23日の国際機械学習会議(ICML)で発表される論文の中で、EquiBindという幾何学的なディープラーニングモデルを開発し、薬剤様分子とタンパク質の結合に成功した際に、既存の最も速い計算分子ドッキングモデルのひとつであるQuickVina2-Wよりも1200倍速くなったと述べている。EquiBindはその前身であるEquiDockをベースにしており、最近MITコンピュータ科学・人工知能研究所のポスドクで、EquiBind論文の共著者でもある故オクタヴィアン=ユージン・ガネアが開発した技術を使って2つのたんぱく質を結合することに特化したモデルとなっている。
「既存の方法は、候補分子のサンプリングとスコアリング、ランク付け、微調整のステップに依存しているため、計算コストが高い…EquiBindは、従来のベースラインや最近のベースラインと比較して、大幅なスピードアップと高い品質を達成した。さらに、既存の微調整技術と組み合わせることで、実行時間の増加という代償を払いながらも、さらなる改善を示している」と著者らは書いている。
ただし、このようなシステムを阻む大きなハードルがある。それは、実験室で作ることが難しい、あるいは不可能な新しい分子構造を、モデルが提案することが多いということだ。化学者が実際にその分子を作ることができなければ、病気と闘う特性をテストすることはできない。
この課題に関してもMITの研究者が、興味深いアプローチを提案している。MITの大学院生のWenhao GaoとポスドクのRocío Mercadoが開発した新しいアプローチは、機械学習モデルを制約し、合成可能な分子構造のみを示唆するようにするものである。この方法では、分子が購入可能な材料で構成され、それらの材料の間で起こる化学反応が化学の法則に従っていることが保証される。
分子構造を作成するために、提案されたモデルは分子を合成するプロセスをシミュレートし、確実に分子を生成できるようにする。モデルには、購入可能な化学物質である「ビルディングブロック」と、有効な化学反応のリストが与えられる。これらの化学反応テンプレートは、専門家が手作業で作成したものだ。これらの入力を制御して、特定の化学物質や特定の反応のみを許可することで、研究者は新しい分子の探索空間の大きさを制限することができる。
このモデルは、これらの入力を使って、ビルディングブロックを選択し、化学反応によってそれらを一度に1つずつ連結してツリーを構築し、最終的な分子を構築していく。各ステップにおいて、化学物質や反応が追加されるため、分子はより複雑になる。
研究者たちは、このモデルを学習させるために、完全な分子構造、構成要素、化学反応のセットを入力する。そしてモデルは、その分子を合成するツリーを作成するように学習する。何十万もの例を見た後、モデルは自ら合成経路を考え出すようになる。
学習させたモデルは、最適化にも利用できる。研究者は、ある種の構成要素と化学反応のテンプレートを使って、最終的な分子で実現したい特性を定義すると、モデルは合成可能な分子構造を提案する。
研究チームは、このモデルが、合成可能な分子をどの程度再現できるかをテストした。その結果、合成可能な分子の51パーセントを再現することができ、それぞれの分子の再現に要した時間は1秒未満であった。
参考資料
Dara, S., Dhamercherla, S., Jadav, S.S. et al. Machine Learning in Drug Discovery: A Review. Artif Intell Rev 55, 1947–1999 (2022). https://doi.org/10.1007/s10462-021-10058-4





