AIはオミクロン株のタンパク質構造をほぼ正確に予測した
ノースカロライナ大学の研究者であるコルビー・フォードは、DeepMindのAlphaFoldとワシントン大学のRoseTTAFoldを用いてシミュレーションを行い、現在のCOVID-19の症例を支配しているオミクロン株のタンパク質構造を予測した。
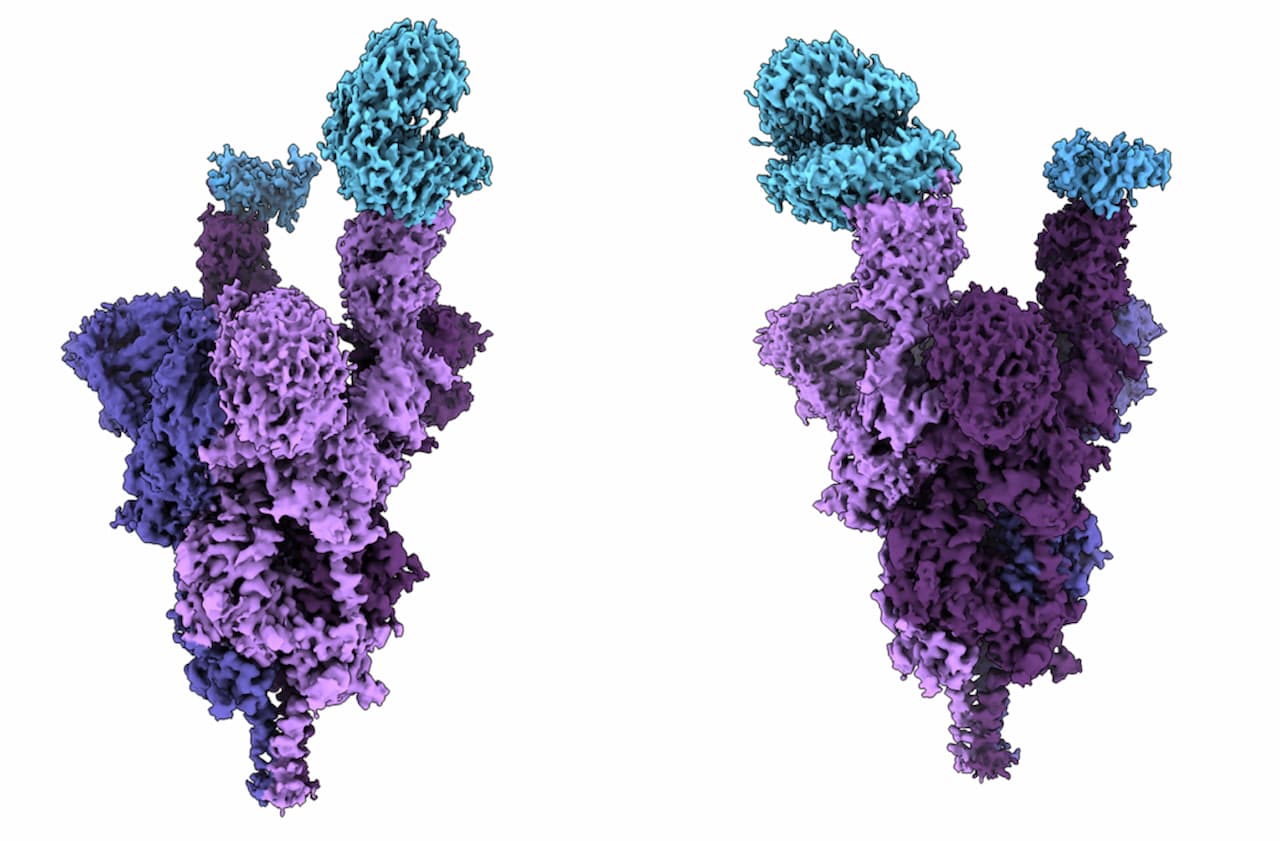
ノースカロライナ大学の研究者であるコルビー・フォードは、DeepMindのAlphaFoldとワシントン大学のRoseTTAFoldを用いてシミュレーションを行い、現在のCOVID-19の症例を支配しているオミクロン株のタンパク質構造を予測した。
12月初旬、フォードと2人の同僚はより詳細な査読なしの論文を投稿した。この論文には、以前の株に対する抗体がオミクロンには効果がないという予測も含まれていた。フォードは、中心となる原子の位置が、水素原子の半径に相当する半オングストローム(0.05nm)ほど異なると計算した。
フォードがこのような結論を出したのは、科学者たちがオミクロン株の実物サンプルを電子顕微鏡で完全に調査し、その構造を正しくマッピングする前のことだった。
カナダのブリティッシュ・コロンビア大学のスリラム・スブラマニアム教授の研究室は、オミクロンのDNAを入手し、その構造を顕微鏡で観察した結果と、実際の抗体を用いたテストの結果を12月下旬に発表した。フォードが予測した2つの構造のうちの1つは、ほぼ正しいことが判明した。フォードは、その中心となる原子の位置が、水素原子の半径に相当する半オングストローム(0.05nm)ほど異なることを計算した。「ツールを使えば、経験に基づく推測を素早く行うことができる。これは、Covidじみた状況では重要なことである。新しいウイルスが登場すれば、私がやったことを他の誰かが再現するだろう」。
カナダのブリティッシュ・コロンビア大学のスリラム・スブラマニアム教授は、「ゴールドスタンダードは常に直接測定することです」と述べている。「もしあなたが10億ドル規模の医薬品プログラムを構築しているなら、人々は何が本物なのかを知りたい」
予測がオミクロンスパイクタンパク質の実験に先行したのは、AIがもたらした最近の分子生物学の大変革を反映している。タンパク質の構造を正確に予測できるソフトウェアが初めて普及したのは、オミクロンが登場するわずか数カ月前のことだった。これは、アルファベット傘下のAI研究所DeepMindとワシントン大学の研究チームが競って開発したものだ。
フォードはこの2つのパッケージを使用したが、どちらもオミクロンじみた突然変異による小さな変化を予測するように設計されておらず、検証もされていなかったため、彼の結果は決定的なものではなく示唆に富んだものだった。研究者の中には、この結果に懐疑的な人もいた。しかし、彼が強力なタンパク質予測AIを簡単に試すことができたという事実は、最近の画期的な技術がすでに生物学者の仕事や考え方を変えつつあることを示している。
スブラマニヤムによると、彼の研究室の成果に向けて作業している間に、オミクロンスパイクの構造予測を提案する人たちから4、5通のメールを受け取ったという。「かなりの数の人が遊び半分でやっていた」と彼は言う。スブラマニアムは、タンパク質の構造を直接測定することが究極の基準であることに変わりはないとしながらも、AIによる予測が将来の病気の発生など、研究の中心になっていくことを期待しているという。
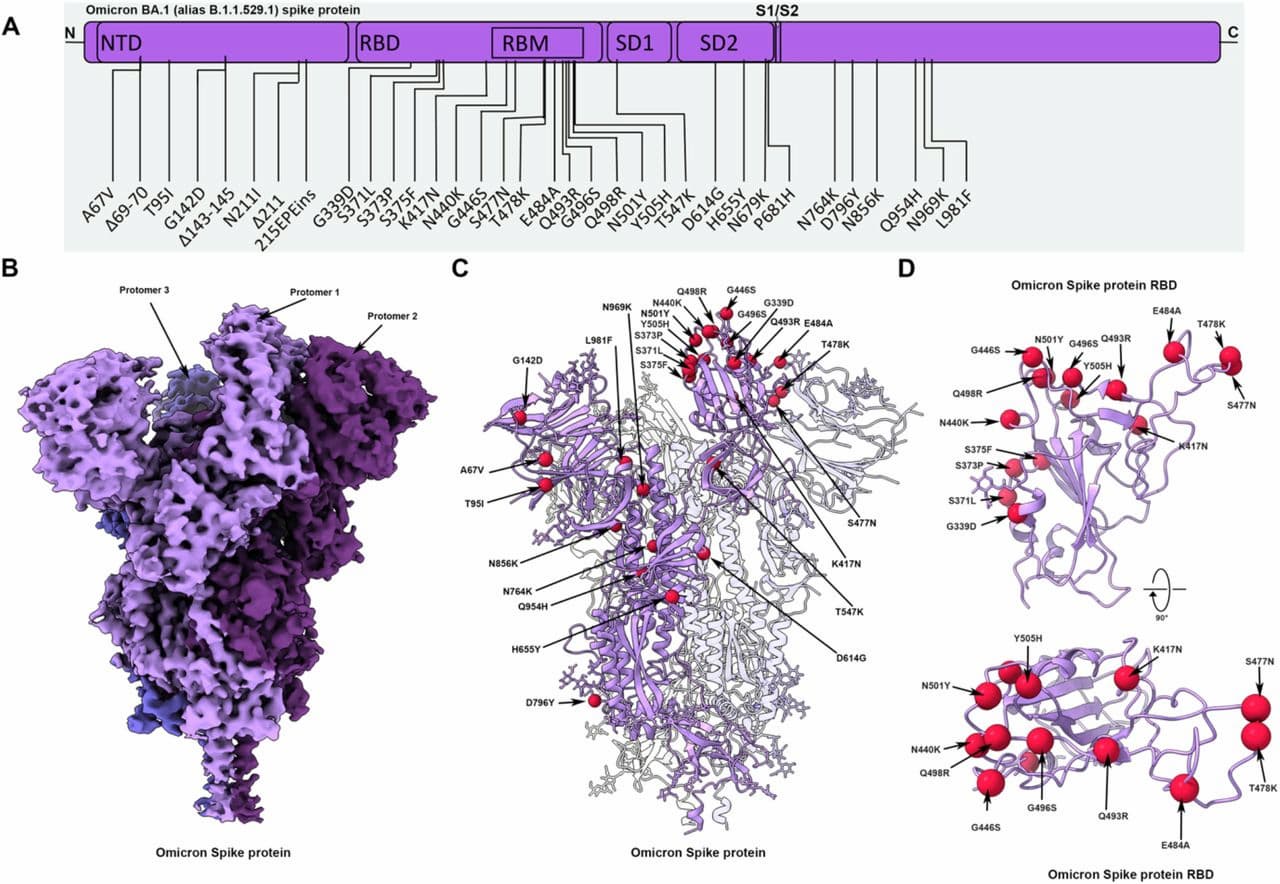
タンパク質はその形によって挙動が決まるため、その構造を知ることは、進化の研究から病気の研究まで、生物学のあらゆる研究に役立つ。医薬品の研究では、タンパク質の構造を解明することで、新しい治療法のターゲットとなる可能性を見出すことができる。
しかし、タンパク質の構造を決めるのは簡単ではあらない。タンパク質は、生物のゲノムにコード化された指示に基づいて組み立てられた複雑な分子であり、酵素や抗体などの生命の仕組みの多くを担っている。タンパク質は、アミノ酸と呼ばれる分子の集まりで、複雑な形に折り畳まれ、さまざまな働きをする。
タンパク質の構造を解明するためには、従来、実験室での骨の折れる作業が必要だった。これまでに知られている約20万種類の構造のほとんどは、タンパク質を結晶にしてX線を照射するという厄介な方法でマッピングされていた。スブラマニヤムが使用した電子顕微鏡じみた新しい技術は、より迅速に行うことができるが、このプロセスはまだ簡単ではない。
2020年後半、アミノ酸配列からコンピュータがタンパク質の構造を予測できるという長年の希望が、数十年にわたる遅々とした進歩を経て、突然現実のものとなった。AlphaFoldと呼ばれるDeepMindのソフトウェアが、タンパク質予測のコンテストで非常に正確であることが証明され、このチャレンジの共同創設者であるメリーランド大学のジョン・モールト教授が問題解決を宣言した。
しかし、この瞬間は、一部の科学者にとってはフラストレーションの溜まるものでもあった。DeepMindは、AlphaFoldがどのように動作するかの詳細をすぐには公表しなかったからだ。
これに対し、ワシントン大学でタンパク質の構造予測を研究しているデイヴィッド・ベイカーは、DeepMindが落とした手がかりをもとに、6月に公開された「RoseTTAFold」というオープンソースソフトウェアの設計を進めた。このソフトウェアは、AlphaFoldと似ているが強力ではない。どちらも、10万以上の既知の構造のコレクションを使って学習し、タンパク質の構造を予測するために磨かれた機械学習アルゴリズムに基づいている。翌月、DeepMindは自らの研究の詳細を発表し、AlphaFoldを誰でも使えるように公開した。これにより、世界にはタンパク質の構造を予測する2つの方法が存在することになったのである。
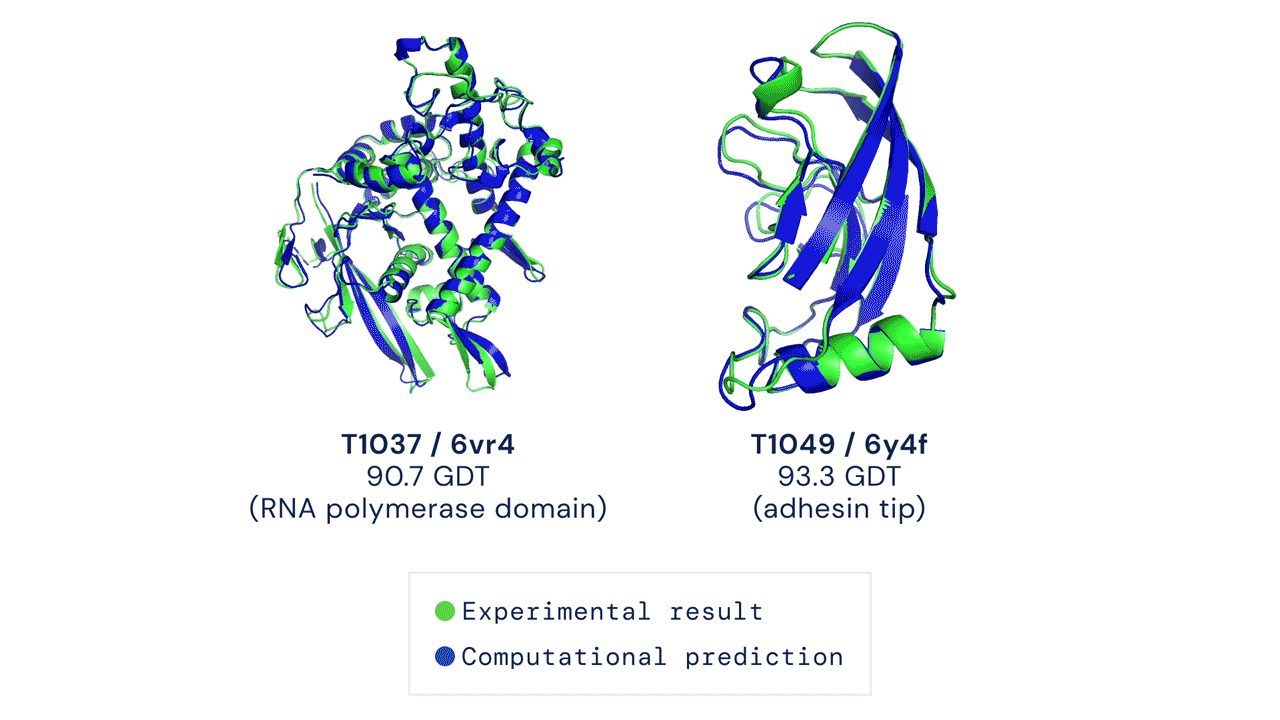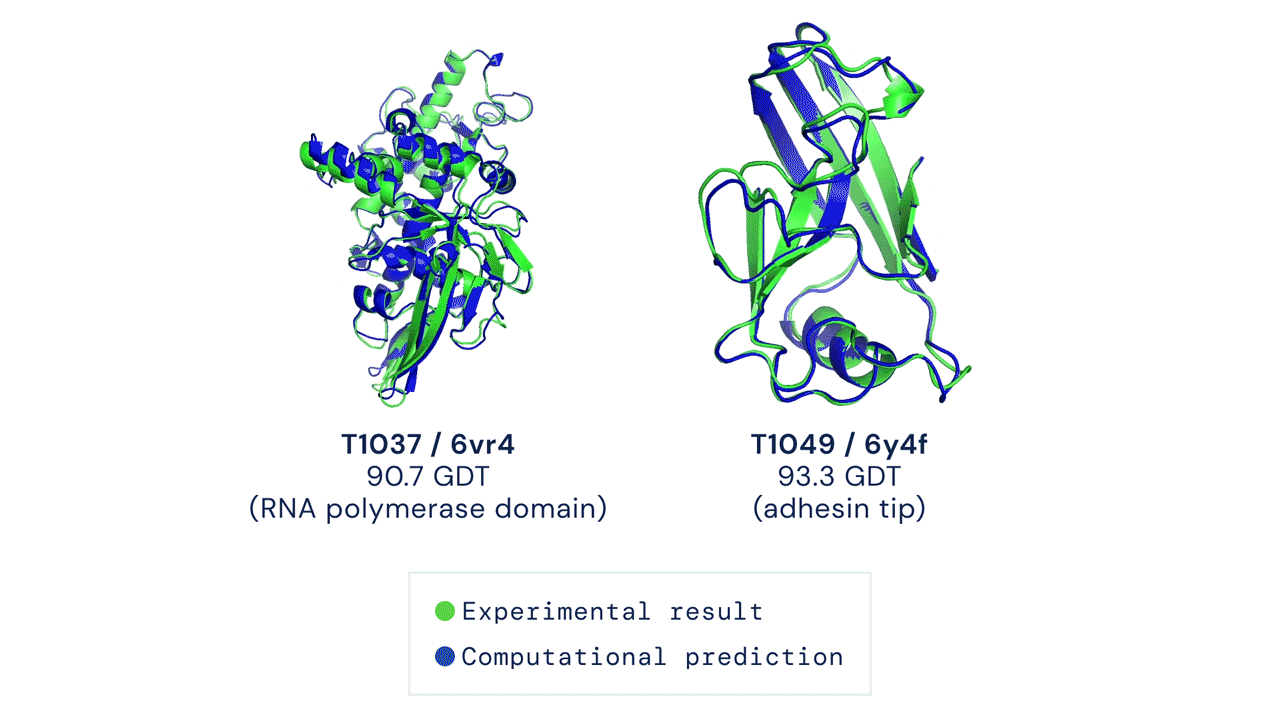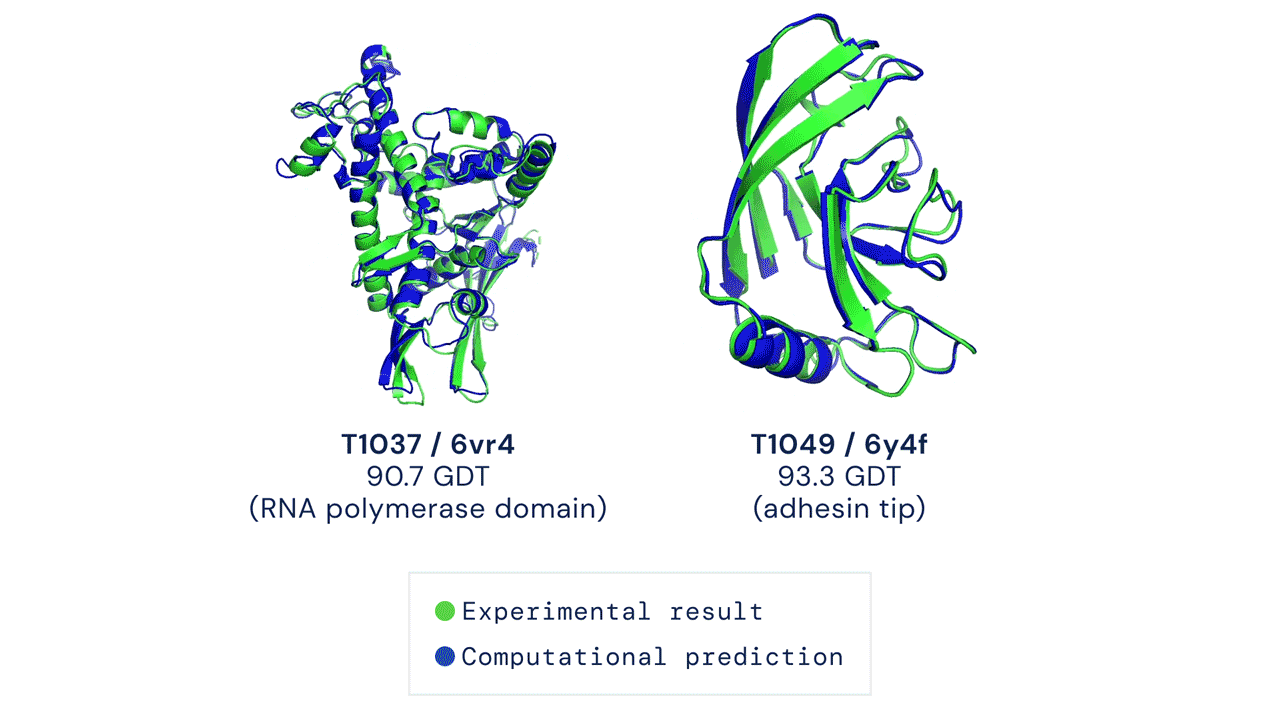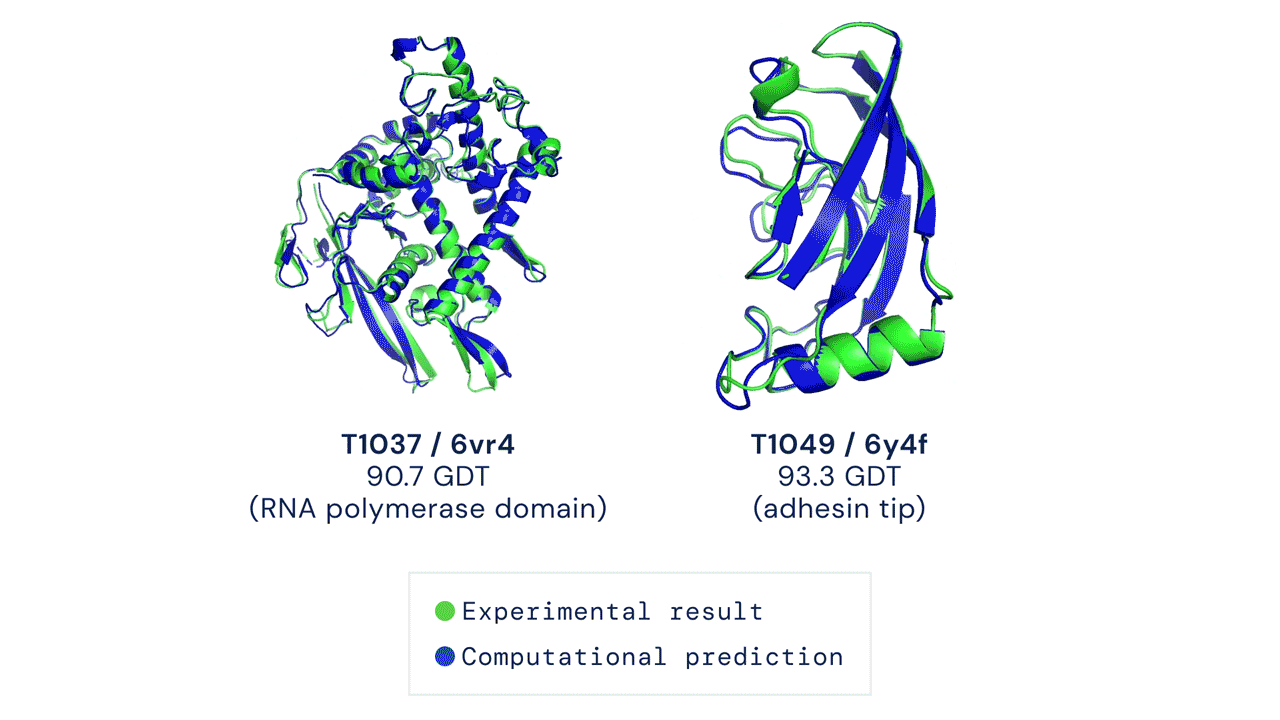
RoseTTAFoldの開発を主導したベイカー研究室のポスドク研究員、Minkyung Baekは、生物学研究においてタンパク質構造予測が標準的なものになるのがいかに早いかに驚いていると言う。Google Scholarによると、UWとDeepMindのソフトウェアに関する論文は、発表されてから短期間で、合わせて1,200以上の学術論文に引用されている。
予測は、コロナウイルス感染症の研究では重要性が証明されていないが、将来の病気への対応ではますます重要になると考えられている。パンデミックを克服する答えがアルゴリズムから完全に導き出されることはにはならないが、予測された構造は科学者が戦略を立てるのに役立つ。実験の労力を最も重要な問題に集中させることもできる。
このように優れた性能を持つタンパク質予測ツールであるが、分子のすべてがわかるわけではない。予測されたタンパク質は、単一の静的な構造を持っており、他の分子と相互作用する際に生じる屈曲やくねりを捉えることはできない。このアルゴリズムは、既知の構造のデータベースで学習されたもので、自然界の多様性というよりは、実験的にマッピングしやすい構造を反映している。
スブラマニアムのオミクロン論文には、スパイクタンパク質の構造に加えて、AIがまだ達成していない種類の結果が含まれている。それは、スパイクが標的とするヒトタンパク質と結合したスパイクの複合構造である。その結果、この変異体の構造の変化により、宿主の細胞とより強く結合することができる一方で、以前の株からの抗体には弱くなっていることが示唆された。これらの組み合わせにより、オミクロンが高度にワクチン接種された地域をも制圧できる理由が説明できるようである。





